 EN
EN
近日,张志超教授课题组连续在药剂学和药物化学领域TOP期刊 《 Journal of Controlled Release》(中科院大类一区,IF = 11.5)和《Journal of Medicinal Chemistry》(中科院大类一区,IF = 6.8)上发表研究,利用分子伴侣蛋白在蛋白质稳态中发挥的分子机器功能,开发了新一代肿瘤特异性、胞内外全域覆盖的精准蛋白降解药物平台,实现了“肿瘤特异性识别+降解机制拓展+降解效率增强”的多重效果。
PROTAC和LYTAC等蛋白靶向降解嵌合体技术分别降解胞内、胞外蛋白,已发展成为小分子药物开发领域的重要研究范式。但是,PROTAC和LYTAC等降解技术机制单一,存在肿瘤选择性不足、无法在同一平台中实现胞内外蛋白的全域降解覆盖、受降解通路上下游事件和“钩状效应”影响导致降解效率受限等问题。热休克蛋白(HSPs)是一类高度保守的分子伴侣蛋白,在蛋白质稳态维持中发挥核心作用。HSP70和HSP90作为表达量和功能互补的核心分子伴侣,在肿瘤细胞中高表达,调控多条不同的蛋白质降解通路——泛素-蛋白酶体(胞内)、内吞-溶酶体(胞外)、自噬-溶酶体途径(胞内)等,为开发高效、肿瘤选择性、全域降解覆盖的新型蛋白降解平台提供了理论依据。
在这两篇论文中,张志超课题组系统解析了伴侣蛋白HSP70和HSP90在肿瘤中的表达量和在蛋白降解中的功能。在表达水平方面,发现HSP70和HSP90均在肿瘤细胞中特异性表达上调,且在不同肿瘤谱系中的表达量具有互补性。在降解功能方面,发现HSP90可在不影响泛素化水平的情况下,通过对“后泛素化”事件的调控,实现与泛素-蛋白酶体降解通路的协同作用,增强PROTAC对胞内蛋白的降解效果;HSP70则通过泛素-蛋白酶体和内吞-溶酶体途径直接识别并降解胞内/外的靶蛋白。基于HSP90和HSP70的天然生物学特征,张志超课题组分别设计了两套蛋白靶向嵌合体系统:
(1)靶向HSP90的生物正交PROTAC前药系统(HBPROTAC),实现PROTAC的肿瘤特异性激活与降解效率增强。HBPROTAC系统由两部分组成:(1)四嗪(Tz)修饰的HSP90抑制剂,可在肿瘤细胞中特异性富集;(2)反式环辛烯(TCO)笼蔽的TCO-PROTAC前药,通过IEDDA反应在肿瘤细胞内点击释放活性PROTAC(如MZ1或DT2216),进而降解靶蛋白(如BRD4或Bcl-xL)。HBPROTAC系统不仅在黑色素瘤小鼠模型中实现了PROTAC在肿瘤部位的特异性激活,显著降低全身毒性,还通过HSP90与泛素化-蛋白酶体降解通路的协同作用,增强了靶蛋白的降解效果。论文链接:https://www.sciencedirect.com/science/article/pii/S0168365926002300
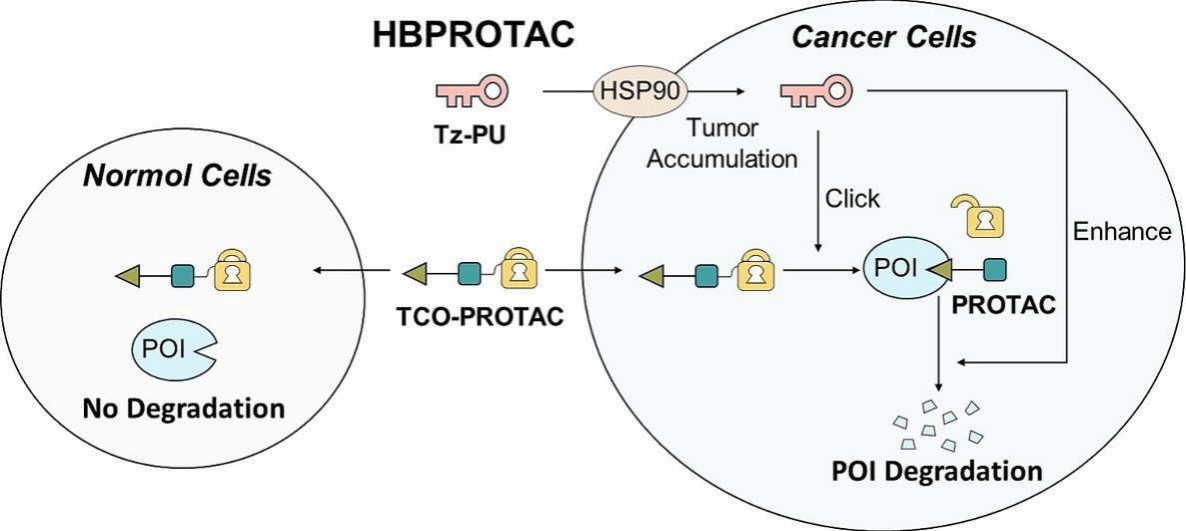
图1. HBPROTAC的机制示意图
(2)基于HSP70的“双通路”肿瘤特异性蛋白靶向降解嵌合体(HSP70TAC)系统,实现单平台对胞内外蛋白的全域降解覆盖。通过将HSP70抑制剂与靶蛋白配体偶联,在一个小分子平台中整合了泛素-蛋白酶体(胞内)和内吞-溶酶体(胞外)双通路,分别降解胞内BRD4与膜蛋白PD-L1,打破了PROTAC在蛋白定位上的“区室化”限制。由于HSP70在肿瘤细胞中丰度高,且HSP70TAC对HSP70亲和力适中(KD ≈ 5 μM),避免了高浓度下三元复合物解离导致的“钩状效应”,保持高效降解。同样,利用Hsp70在肿瘤细胞中高表达的特征,Hsp70TAC也能够实现对靶蛋白的肿瘤特异性降解,降低正常细胞毒性。论文链接:https://pubs.acs.org/doi/10.1021/acs.jmedchem.5c03784
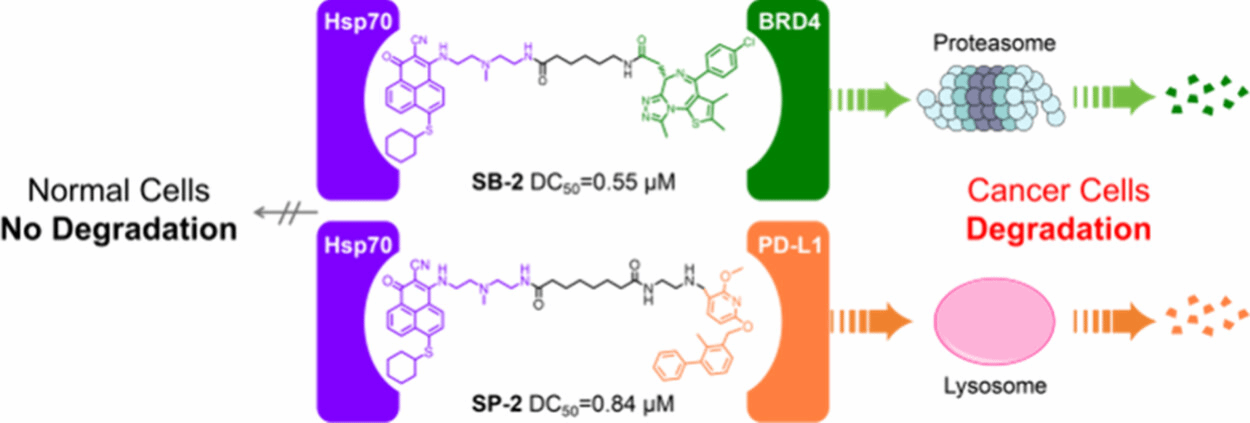
图2. HSP70TAC的机制示意图
这两类蛋白降解系统在适用的肿瘤类型上具有互补性:HSP70TAC和HBPROTAC分别适用于Hsp70和Hsp90高表达的肿瘤,共同构建了一个覆盖更广泛肿瘤谱系、机制互补、模块化设计的PROTAC技术平台。
博士生殷方奎、硕士生王子涵分别为两篇论文的第一作者,医学部王紫千副教授、张志超教授为通讯作者。该工作得到了国家自然科学基金面上项目、大连理工大学基础研究挂帅揭榜项目、大连理工大学-附属中心医院、附属肿瘤医院、附属第三人民医院医工合作项目的资助。